|
|
|
|
|
|
Телефон: (8-352-22) 3-64-65, Факс: 3-63-54 Телефон домашний: (8-352-22) 6-53-03 |
|
|
|
|
|
|
Телефон: (8-352-22) 3-64-65, Факс: 3-63-54 Телефон домашний: (8-352-22) 6-53-03 |
ЧРЕСКОСТНЫЙ КОМПРЕССИОННО-ДИСТРАКЦИОННЫЙ ОСТЕОСИНТЕЗ В ОРТОПЕДИЧЕСКОЙ РЕАБИЛИТАЦИИ БОЛЬНЫХ С ПЕРВИЧНЫМИ ОПУХОЛЯМИ ДЛИННЫХ ТРУБЧАТЫХ КОСТЕЙ
И.И.БАЛАЕВ
Областной онкологический диспансер г.Курган (Главный врач Т.И.Сиротская)
При хирургическом лечении
опухолей костей должны быть
соблюдены следующие
основные принципы:
радикальный характер
операции….., абластичность…..,
сохранение… конечности ...
без нарушения ее функции
Академик Н.Н.Трапезников
Первичные опухоли костей встречаются сравнительно редко и составляют 1-4% в общей структуре всех онкологических заболеваний человека, но по тяжести патологии это один из трудных в диагностическом и лечебном плане разделов клинической онкологии. В большинстве случаев они возникают у детей и лиц молодого возраста и в 70-80% лока-лизуются в длинных трубчатых костях. В настоящее время для лечения костных опухолей с учетом их гистогенеза применяются хирургический, лучевой и лекарственный методы лечения. Однако, для большинства больных хирургический метод лечения является ос-новным и занимает главное место в комплексном лечении, а при доброкачественных опу-холях единственно эффективным.
В хирургическом методе лечения опухолей костей по показаниям применяются как калечащие (ампутация, экзартикуляция), так и сохранные (резекция) операции. Органо-сохраняющие операции - это новое и передовое научно-практическое направление в со-временной онкологии и восстановительной хирургии. В них тесно взаимосвязано решение задач ликвидации патологического процесса и адекватного замещения образующегося после операции дефекта кости для обеспечения опорнодвигательной функции конечности. Cреди современных методов реконструктивно-восстановительной хирургии при дефектах длинных костей различной величины и локализации чрескостный остеосинтез имеет значительные преимущества в отношении полноты замещения дефекта и возможности рациональной реконструкции поврежденной конечности. Представляет несомненный интерес тот факт, что, получая все большее распространение в ортопедии и травмато-логии, метод чрескостного компрессионно-дистракционного остеосинтеза практически не использовался в онкологии, несмотря на то, что сохранные операции при опухолях костей стали все шире использоваться в онкологической клинике. Лишь в последнее десятилетие появились сообщения об использовании метода чрескостного компрессионно-дистракционного остеосинтеза при хирургическом лечении больных с первичными опухолями длинных трубчатых костей. Однако, данные работы основаны на сравнительно небольшом опыте использования методик чрескостного остеосинтеза в данной проблеме и отражают лишь некоторые клинические аспекты и результативность его применения. Представленная в них информация не позволяет обьективно с позиций углубленного анализа провести сравнительную оценку применяемых методик, их вариантов и уточнить дифференцированные показания к их применению с учетом детализированной специфики лечения больных с доброкачественными и злокачественными опухолями костей. Поэтому не представляется возможным извлечь из существующих работ конкретные практические рекомендации по применению чрескостного остеосинтеза в костной онкологии. Нами на-коплен значительный клинический опыт успешного применения чрескостного остеосинтеза по Илизарову в реабилитации больных с первичными опухолями длинных трубчатых костей. Поэтому многофакторное обобщение, детальная систематизация клинического материала с выработкой дифференцированных рекомендаций по применению отдельных методик и их вариантов в системе восстановительного лечения пациентов с этой тяжелой формой костной патологии является высоко актуальным.
Материал основан на анализе опыта применения чрескостного остеосинтеза при лечении 72 больных с первичными опухолями трубчатых костей костей. В возрасте до 30 лет было 76,2% пациентов, дети и подростки составили 28,9%. По гистологическому строе-нию у 47 (65,2%) больных были доброкачественные новообразования: гигантоклеточная опухоль - 38 (52,7%), хондрома - 4 (5,5%), хондробластома - 2 (2,8%), хондромиксоидная фиброма - 2 (2,8%), десмопластическая фиброма - 1 (1,4%). У 25 (34,8%) больных выяв-лена злокачественная опухоль: остеогенная саркома - 11 (15,3%), юкстакортикальная ос-теосаркома - 2 (2,8%), злокачественная фиброзная гистиоцитома - 7 (9,7%), ретикулосар-кома - 2 (2,8%), саркома Юинга - 1 (1,4%), фибросаркома - 1 (1,4%), <<адамантинома >> длинных костей - 1 (1,4%). Из 47 больных с доброкачественной опухолью у 20 она пора-жала бедренную кость, у 22 большеберцовую и у 5 - плечевую и лучевую кости. Из 25 пациентов со злокачественной опухолью у 5 была поражена бедренная кость, у 16 - больше-берцовая , у 1 - плюсневая кость и у 3 - плечевая кость. Наиболее типичной локализацией новообразований была область метаэпифиза, причем чаще поражались кости, образующие коленный сустав - у 39 (54,1%) больных от общего числа пациентов.
(Распределение больных со злокачественными опухолями в зависимости от хирурги-ческой стадии заболевания по Enneking W.F., et al. представлено в таблице 1.
Из таблицы - 1 видно, что у 15 (60,0%) больных размеры опухоли выходили за пределы одной анатомической структуры, опухоль обладала высокой степенью злокачественности, а у двух пациентов имелся регионарный или отдаленный метастаз. Все это затрудняло выполнение сохранных операций у этой группы больных и ухудшало отдаленный прогноз лечения
C учетом показаний 19 (76,0%) больным со злокачественными опухолями костей (ос-теогенная саркома - 11, злокачественная фиброзная гистиоцитома - 5, ретикулосаркома - 2, cаркома Юинга - 1) была проведена неоадьювантная химиотерапия, согласно методикам разработанным в РОНЦ им. Н.Н.Блохина РАМН , а трое пациентов в предоперационном периоде получили и лучевую терапию с суммарной очаговой дозой 36 грей. Эффек-тивность проведенного в предоперационном периоде химиолучевого лечения оценивали по степени лечебного патоморфоза опухоли согласно схеме предложенной Huvos A.G., et al. У 9 (47,3%) пациентов была достигнута 3 степень лечебного патоморфоза опухоли, у 10 (52,7%) установлена - 1 - 2 степень.Пострезекционные дефекты кости составили от 5 до 27 см. Для их замещения были применены варианты моно- и полилокального удлинения отломков, смежных сегментов и межкостного синостозирования, разработанный вариант свободной аутопластики в сочетании с чрескостным остеосинтезом при околосуставной локализации доброкачественной опухоли и свободной аутопластики трубчатым фрагментом малоберцовой кости для за-мещения тотального и субтотального дефекта плечевой кости при злокачественной опухоли. C целью оптимизации условиий и повышения эффективности реконструктивно-восстановительного лечения предложены новые технические решения, защищенные авторскими свидетельствами (а.с. 1168229) и 2 заявками на выдачу патента РФ (заявка 93052252, приоритет от 16.11.93г. ;заявка 94006637, приоритет от 22.03.94г.). Динамика репаративного костеобразования в период лечения была изучена методами ос-теосцинтиграфии и двухфотонной абсорбциометрии (рис.1) и свидетельствовала об акти-визации обменных процессов в костной ткани при замещении пострезекционных дефек-тов путем формирования дистракционного регенерата. При этом отмечено, что минерали-зация регенератов быстрее происходит при замещении дефектов после удаления доброка-чественных опухолей и медленнее - злокачественных. Однако такая тенденция отмечается на 1-3 месяце дистракции, а к концу ее и началу фиксации процесс минерализации происхо-дит однонаправленно.
Анализ результатов лечения проводился дифференцированно, с учетом общеприня-тых онкологических принципов и по критериям анатомо-функциональной реабилитации. В группе больных (47) с доброкачественными опухолями рецидивов не было. Анализ вы-живаемости больных (25) со злокачественными опухолями показал, что она соответство-вала средним статистическим данным мировой литературы, составила в течение трех лет 68,4% и была пятилетней у 46,6% лечившихся. Оценка анатомо-функциональных исходов ортопедической реабилитации показала, что методики были эффективны у 94,6% пациен-тов закончивших лечение. C целью иллюстрации эффективности разработанных методик лечения приводим два клинических наблюдения.
Наблюдение 1. Больной К., 5 лет, ист. бол. 1180/352. Поступил на лечение в облон-кодиспансер г.Кургана с жалобами на наличие опухоли и ноющие боли после физической нагрузки в нижней трети правого бедра. Год назад при пальпации была обнаружена опухоль в нижней трети правой бедренной кости. Данные рентгенографии и трепанобиопсии опухоли показали картину юкстакортикальной остеосаркомы. В онкодиспансере по месту жительства пациенту провели 1 курс полихимиотерапии (адриамицин, циклофосфан, винкристин, сарколизин) и дистанционную гамма-терапию с СОД в 36 грей. От предло-женной ампутации конечности родители ребенка отказались.
При поступлении в нижней трети правого бедра обнаружена опухоль костной конси-стенции, исходящая из бедренной кости, размерами 4х4 см, умеренная атрофия мышц бедра и голени. Объем движений в коленном суставе ограничен за счет сгибания до угла 90º. На рентгенограммах (рис.2) в дистальном метадиафизе правой бедренной кости опре-деляется очаг деструкции дольчатого строения, округлой формы плотно прилегающий к корковому слою кости. Размеры новообразования 3,5х1,5 см. Диагноз: юкстакортикальная остеосаркома дистального метадиафиза правой бедренной кости. Повторное гистологиче-ское исследование микропрепаратов трепанобиопсии опухоли подтвердило ранее уста-новленный диагноз юкстакортикальной остеосаркомы. Приняли решение после сегмен-тарной резекции дистального метадиафиза правой бедренной кости операционный дефект заместить с помощью применения методики монолокального последовательного компрес-сионно-дистракционного остеосинтеза.
Под перидуральной анестезией выполнили операцию по планируемой методике (рис.4). Величина послеоперационного дефекта дистального метадиафиза правой бедренной кости составила 5 см. Гистологическое исследование препарата удаленной опухоли показало картину юкстакортикальной остеосаркомы (рис.4). Послеоперационный период протекал гладко. В течение 12 дней в зоне стыка нижнего края проксимального отломка бедренной кости с верхним краем дистального поддерживали стабильную компрессию. В дальней-шем в зоне стыка концов отломков выполняли дистракцию, которую продолжали 75 дней до устранения операционного дефекта кости (рис.4; рис.5). Последующая фиксация ко-нечности аппаратом длилась 8 месяцев. Достигнуто восстановление анатомической цело-стности и длины бедренной кости с сохранением ростковых зон. При обследовании через 5 лет рецидива опухоли нет. Пациент ходит без вспомогательных средств опоры, учится в шко-ле (рис.6).
Наблюдение 2. Больная Г., 11 лет , ист. бол. 1758/923. Поступила на лечение в ООД г.Кургана с жалобами на переодические ноющие боли в левой голени и наличие опухоли. При осмотре по передней поверхности левой голени в проекции проксимального мета-эпифиза большеберцовой кости обнаружена опухоль эластической консистенции, болез-ненная при пальпации, размерами 4х3 см. Объем движений в коленном суставе ограничен за счет сгибания. Умеренная атрофия мышц бедра и голени. На рентгенограмме (рис. 6) определяется очаг деструкции костной ткани в проксимальном метаэпифизе левой боль-шеберцовой кости в виде очагов остеосклероза размерами 5х3 см, по передней поверхности периостальный козырек Кодмана. Диагноз: остеогенная саркома проксимального ме-таэпифиза левой большеберцовой кости. Данные биопсии опу-холи подтвердили клинико-рентгенологический диагноз остеогенной саркомы. Учитывая морфологическое строение опухоли, ее локализацию и размер, возраст пациентки, приняли решение провести не-оадьювантную химиотерапию и выполнить органосохраняющую операцию в объеме сег-ментарной резекции проксимального суставного конца большеберцовой кости. Операци-онный дефект заместить путем удлинения дистального отломка с созданием тибиофемо-рального синостоза, применив методику билокального последовательного дист-ракционно-компрессионного остеосинтеза. Больной в интервале 3 недели провели два курса внутри-артериальной инфузии адриабластина суммарной дозой 200 мг. В реультате лечения ку-пировался болевой синдром, отмечено уменьшение мягкотканного компонента опухоли. Через 2 недели под перидуральной анестезией выполнили операцию по запланированной методике (рис.9). Длина послеоперационного дефекта проксимального суставного конца левой большеберцовой кости составила 13 см. Гистологическое исследование препарата показало картину остеогенной саркомы, остеопластический вариант, лечебный патоморфоз опухоли 3 степени (рис.10). Послеоперационный период протекал без осложнений. Через неделю стали перемещать остеотомированный фрагмент дистального отломка большеберцовой кости в сторону операционного дефекта (снизу вверх). Дистракцию продолжали в течение четырех месяцев до стыка перемещенного фрагмента с нижним краем бедренной кости. Последующая фиксация конечности в аппарате продолжалась 8 месяцев (рис.11). Восстановлена опороспособная функция конечности с созданием тибиофемо-рального синостоза. Одновременно с замещением дефекта кости провели семь курсов по-слеоперационной химиотерапии в режиме предоперационной. Общая доза адриабластина с учетом предоперационной химиотерапии составила 920 мг. Через 2 года в процессе рос-та пациентки установили отставание темпа роста оперированной конечности на 5 см. Укорочение конечности устранили путем удлинения голени на одном уровне. Осмотрена через 10 лет после операции. Жалоб нет, ходит свободно без вспомогательных средств опоры. На контрольных рентгенограммах (рис.12) определяется целостность большебер-цовой кости, тибио-феморальный синостоз, рецидива опухоли нет.
В обоих приведенных наблюдениях метод был применен у пациентов детского воз-раста с незавершенным формированием скелета, а это по данным как отечественных так и зарубежных авторов является противопоказанием к выполнению органосохраняющих операций в связи с тем, что использование в этих случаях классических методов пластики (ауто-, аллопластика, эндопротезирование) приводит к значительному отставанию темпа роста оперированной конечности и развитию ее функциональной несостоятельности.
Таким образом, наш опыт применения чрескостного остеосинтеза при лечении больных с первичными опухолями костей показывает, что метод высокоэффективен, по-зволяет замещать операционные дефекты кости и осуществлять оптимальную реконст-рукцию конечности не только у взрослых, но и у детей с незавершенным формированием скелета. У больных с саркомой кости с учетом показаний метод целесообразно использо-вать после предварительного этапа, включающего радикальную и абластичную резекцию опухоли с соответствующим комплексом неоадьювантной химиитерапии. При резекции доброка-чественных опухолей реабилитационные мероприятия по анатомо-функциональному восстановлению оперированной конечности должны выполняться в один этап.
,
Таблица и рисунки и к статье И.И.Балаева
ЧРЕСКОСТНЫЙ КОМПРЕССИОННО-ДИСТРАКЦИОННЫЙ ОСТЕОСИНТЕЗ В ОРТОПЕДИЧЕСКОЙ РЕАБИЛИТАЦИИ БОЛЬНЫХ С ПЕРВИЧНЫМИ ОПУХОЛЯ-МИ ДЛИННЫХ ТРУБЧАТЫХ КОСТЕЙ
Таблица 1
Распределение больных с костными саркомами в зависимости от хирургической стадии заболевания
|
Нозология\ Стадия |
I A |
I B |
II A |
II B |
III |
Всего |
|
Остеогенная саркома |
1 |
1 |
2 |
6 |
1 |
11 |
|
Юкстакортикальная остеосаркома |
2 |
- |
- |
- |
- |
2 |
|
Фибросаркома |
- |
- |
1 |
- |
- |
1 |
|
Злокачественная фиброзная гис-тиоцитома |
1 |
1 |
- |
4 |
1 |
7 |
|
Ретикулосаркома |
- |
- |
- |
2 |
- |
2 |
|
Саркома Юинга |
- |
- |
- |
1 |
- |
1 |
|
«Адамантинома» длинных костей |
- |
- |
1 |
- |
- |
1 |
|
ВСЕГО |
4 |
2 |
4 |
13 |
2 |
25 |
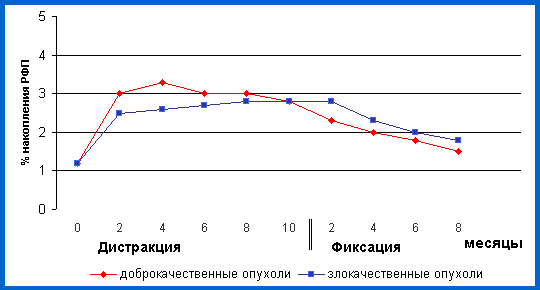
Рис.1. Динамика накопления меченого технефора в регенерате при замещении дефектов кости после резекции доброкачественных и злокачественных опухолей
|
|
Рис.2. Рентгенограммы больного К. до лечения |
|
|
Рис. 3. Микрофотограмма препарата больного К. Юкстакортикальная остесаркома .(окраска гематоксилином, эо-фином х 63). |
|
|
Рис. 4. Рентгено-граммы больного К., после операции |
|
Рис. 5. Рентгено-граммы больного К., в процессе ди-стракции |
|||
|
|
|
|
Рис. 6. Рентгенограммы и больной К., через 5 лет после снятия аппарата |
|||
|
|
Рис.7. Рентгенограммы больной Г., до лечения |
|
|
Рис.8. Микрофотограмма препарата больной Г.. Остеогенная саркома, лечебный патоморфоз III степени (окраска гематоксилином, эози-ном х 63) |
|
|
|
Рис.9. Рентгенограммы больной Г., после операции и в процессе лечения |
|
|
Рис.10. Рентгенограммы больной Г., через 9 лет после операции
|